Ana Flávia Lopes Santos1
Grazielle Souza Damasceno1
Vanessa Cristina Fernandes1
Thayná Marcele Martins Guedes1
Wesley Ribeiro Soares2
Vinícius Santos da Silva3
Adriana Nascimento de Sousa4
Gilson de Freitas Silva5
Ynara Marina Idemori5
Sérgio Fernando de Oliveira Gomes6
Eliane do Nascimento7
.
Resumo: A poluição ambiental, decorrente da geração de resíduos, tem aumentado com o progresso tecnológico e com o aumento populacional. Destacam-se, neste contexto, os resíduos decorrentes da rotina de indústrias químico-farmacêuticas e, principalmente, o descarte indevido de fármacos e de seus metabólitos ativos na rede de esgoto doméstico. Dentre os inúmeros fármacos potencialmente poluentes do meio ambiente destaca-se o hormônio 17a-etinilestradiol devido ao seu efeito impactante no ciclo de vidas de diversos seres vivos. Uma alternativa sustentável para a diminuição da contaminação do ambiente, principalmente do solo e das águas, é o uso de catalisadores que promovam a degradação destes poluentes. As metaloporfirinas são uma classe de compostos macrocíclicos de ocorrência natural que exercem um papel muito importante no metabolismo de organismos vivos, sendo promissoras para aplicação como catalisadores nas reações de degradação de fármacos como, por exemplo, o 17a-etinilestradiol. O estudo do potencial catalítico dessas metaloporfirinas na degradação de fármacos e de seus metabólitos ativos requer a utilização de técnicas analíticas apropriadas. A técnica mais comumente relatada na literatura para análises de 17a-etinilestradiol e de seus correlatos é cromatografia líquida de alta eficiência (CLAE). Visando estudar o grau de degradação do 17a-etinilestradiol promovido por metaloporfirinas em sistemas oxidativos e determinar seus produtos de degradação, foram desenvolvidas as condições cromatográficas adequadas para as análises por CLAE.
Palavras-chave: 17a-Etinilestradiol. Metaloporfirina. CLAE.
.
Abstract: Environmental pollution arising from waste generation has increased with technological progress and population growth. Noteworthy in this context, waste resulting from routine chemical-pharmaceutical industries and, especially the improper disposal of drugs and their active metabolites in domestic sewage network. Among the numerous drugs potentially polluting the environment stands out because of the hormone 17a-ethinylestradiol effect impacting the cycle lives of many living beings. A sustainable alternative to reduce contamination of the environment, especially soil and water is the use of catalysts that promote the degradation of these pollutants. Metalloporphyrins are a class of naturally occurring macrocyclic compounds which have a very important role in the metabolism of living organisms being promising for use as catalysts in degradation reactions to drugs, such as 17a-ethinylestradiol. The study of the catalytic potential of these metalloporphyrins degradation of drugs and their active metabolites requires the use of appropriate analytical techniques. The technique most commonly reported in the literature for the analysis of 17a-ethinylestradiol and its correlates is high performance liquid chromatography (HPLC). To study the rate of degradation of 17a-ethinylestradiol promoted by metalloporphyrins systems and determine their oxidative degradation products, were developed chromatographic conditions appropriate for analysis by HPLC.
Keywords: 17a-Ethinylestradiol. Metalloporphyrin. HPLC.
.
INTRODUÇÃO
A poluição ambiental é um tema preocupante em todo o mundo. Nos últimos anos, esse assunto vem sendo alvo de diversas discussões e uma delas é sobre a poluição das águas e dos solos através da excreção humana de fármacos e seus metabólitos que não são totalmente removidos nas Estações de Tratamento de Esgoto (ETEs) (BILA; DEZOTTI, 2003; COLLINS; BRAGA; BONATO,1997).
Outras causas de contaminação do meio ambiente por fármacos são os medicamentos de uso veterinário usados em larga escala e o descarte indevido de medicamentos em desuso pela população que, geralmente, o faz na rede de esgoto residencial (COLLINS; BRAGA; BONATO, 1997).
Observa-se que a ocorrência de fármacos residuais no meio ambiente acarreta danos, principalmente, em ambientes aquáticos. No entanto, existem poucos estudos sobre esse tema (THORPE et al.,2003; PICKERING; SUMPTER, 2003). Assim, há uma busca intensa por métodos viáveis para a eliminação eficiente destes poluentes pela comunidade científica. Neste contexto, catalisadores porfirínicos mostram-se como candidatos promissores à degradação destes resíduos (MAKARSKA; RADZKI; LEGENDZIEWICZ, 2002).
As porfirinas pertencem à classe dos compostos macrocíclicos de ocorrência natural que exercem um importante papel no metabolismo de organismos vivos. Entre os principais representantes deste grupo de macrociclos tetrapirrólicos destacam-se os complexos de ferro nas hemoproteínas e nos citocromos P-450 (metaloporfirinas), os derivados de magnésio nas clorofilas (metaloclorinas) e os de cobalto na vitamina B12 (metalocorrina), que exercem funções essenciais em processos biológicos como a fotossíntese, o transporte e estocagem de oxigênio, o transporte de elétrons e catálise, entre outras (MILGROM, 1997).
Desde o surgimento do primeiro sistema artificial envolvendo uma metaloporfirina sintéticacomo catalisador em reações de oxidação de substratos orgânicos por iodosilbenzeno (PhIO) (GROVES; NEMO; MEYERS, 1979), vários sistemas oxidativos catalisados por metaloporfirinas foram desenvolvidos (MEUNIER, 1992; BIESAGA et al., 2000; MANSUY, 2007; HUANG; LI; WANG, 2010).
Para a aplicação de metaloporfirina como catalisador da reação de degradação oxidativa do hormônio 17a-etinilestradiol, um dos fármacos potencialmente poluente do meio ambiente, foi necessário desenvolver a metodologia analítica adequada para as análises desse hormônio, do seu grau de degradação, bem como, dos seus produtos de degradação.
De acordo com os relatos na literatura, a técnica analítica mais utilizada para as análises envolvendo hormônios é a cromatografia líquida de alta eficiência (CLAE) devido a sua alta sensibilidade e seletividade, além de ser conhecida como um dos mais eficientes e modernos métodos de separação existentes (ANVISA, 2002). A CLAE é utilizada para separar compostos de alto peso molecular, substâncias pouco voláteis e materiais termicamente instáveis. Pode ainda ser empregada nas separações de elementos em baixíssimas quantidades em misturas complexas, fornecendo resultados rápidos, exatos e precisos. Além disso, permite análises multielementares em uma única injeção com alta resolução, sensibilidade e seletividade, para as quais necessita de apenas alguns microlitros de amostra (ANVISA, 2002). Além disso, os diversos tipos de detectores, colunas e composições de fase móvel permitem que a análise por CLAE se estenda a vários tipos de analitos (COLLINS; BRAGA; BONATO, 1997).
Assim, a grande versatilidade da CLAE foi a base para a sua utilização como a técnica analítica principal para os estudos de degradação do hormônio 17a-etinilestradiol catalisado por metaloporfirina.
.
METODOLOGIA
Para a determinação da metodologia analítica a ser utilizada para as análises do hormônio 17α-etinilestradiol e de seus correlatos 17β-estradiol, estriol e estrona, por CLAE foram feitos levantamentos bibliográficos das condições comumente utilizadas. Após as pesquisas realizadas, foram programados vários testes para definir a fase móvel a ser utilizada, a velocidade do fluxo da fase móvel e o tempo de eluição das amostras injetadas. Todos os testes foram realizados à temperatura ambiente, injetando-se automaticamente 40 mL de amostra e utilizando-se a coluna cromatográfica de fase estacionária de octadecilsilano (Shimadzu C18, 250mmx5mm, 5mm) para sistema cromatográfico de fase reversa, utilizando um aparelho de CLAE com detector de UV-Vis (Agilent 1100 Series).
As soluções estoque contendo os hormônios 17α-etinilestradiol (Sigma-Aldrich, 99,5%), 17β-estradiol (Sigma-Aldrich, 99,9%), estriol (Sigma-Aldrich, 98,0%) e estrona (Sigma-Aldrich, 99,0%) nas concentrações de 0,1 mg/mL foram preparadas individualmente em balões volumétricos de 50,00 mL utilizando-se metanol grau HPLC (Baker) como solvente. Foram pesados 5,0 mg de estrona (18,5 µmol), 5,0 mg de 17α-etnilestradiol (16,9 µmol), 5,0 mg de estriol (17,3 µmol) e 5,0 mg de 17β-estradiol (18,4 µmol) em uma balança analítica (Sartorius) e transferidos quantitativamente para balões volumétricos de 50,00 mL e os volumes completados com metanol grau HPLC.
Foram retiradas alíquotas das soluções estoque dos hormônios e filtradas em filtro seringa (Millex PTFE 25 mm, 0,45 µm). Mediu-se exatamente 0,250 mL de cada solução, utilizando-se microseringa (Hamilton, 250 mL), e transferiu-se para um vial de 1,5 mL de capacidade com tampa de rosca e septo de teflon, obtendo-se uma mistura dos hormônios na concentração de 0,025 mg/mL. Essa mistura de hormônios foi utilizada nos testes para determinação da fase móvel do sistema, da velocidade do fluxo da fase móvel e do tempo de eluição das amostras injetadas.
Para determinar a velocidade do fluxo da fase móvel partiu-se de um fluxo de 1,0 mL/min que foi ajustado para 0,8 mL/min. Concomitantemente, variou-se a fase móvel e o tempo de análise, partindo-se de uma fase móvel constituída da mistura de metanol grau HPLC e água purificada (Mili-Q) na proporção de 50:50. Em seguida, substituiu essa mistura pela mistura de acetonitrila grau HPLC (Baker) e água purificada nas proporções de 40:60; 60:40 e, finalmente, 50:50, obtendo-se tempos de análise que variaram de 30 minutos a 2 horas.
Após ter realizado a escolha das melhores condições cromatográficas para as análises dos hormônios, elaborou-se uma curva de calibração para o 17a-etinilestradiol para avaliar a linearidade das áreas dos picos nos cromatogramas obtidos em função das diferentes concentrações de 17a-etinilestradiol injetadas. Para isto, foi preparada uma solução estoque de 17a-etinilestradiol na concentração de 0,2 mg/mL em metanol grau HPLC. Foram preparadas soluções diluídas a partir da solução estoque nas concentrações de 0,02 mg/mL; 0,04 mg/mL; 0,06 mg/mL; 0,08 mg/mL; 0,09 mg/mL; 0,10 mg/mL; 1,10 mg/mL; 1,20 mg/mL. Alíquotas de 40 mL dessas soluções foram injetadas automaticamente e individualmente pelo equipamento de CLAE em triplicata, utilizando-se para eluição a fase móvel constituída da mistura de acetonitrila grau HPLC e água purificada (50:50) com fluxo de 0,8 mL/min, coluna cromatográfica com fase estacionária C18, à temperatura ambiente, com tempo de análise de 30 minutos.
.
RESULTADOS E DISCUSSÃO
As condições cromatográficas adequadas para as análises do hormônio 17a-etinilestradiol e de seus correlatos 17b-estradiol, estriol e estrona, por CLAE foram determinadas com o objetivo de serem aplicadas nos estudos de reações de degradação oxidativa do 17a-etinilestradiol catalisadas por metaloporfirina.
Os testes para obtenção das melhores condições de análise por CLAE foram realizados, utilizando-se uma mistura dos hormônios 17a-etinilestradiol, estriol, estrona e 17-estradiol, obtidos comercialmente com altos teores de pureza, em solução de metanol grau HPLC a 0,025 mg/mL. A mistura dos hormônios foi analisada em diferentes comprimentos de onda: 280 nm, 240 nm, 230 nm, 220 nm, e 205 nm, sendo que os picos dos cromatogramas apresentaram melhor resolução em 280 nm.
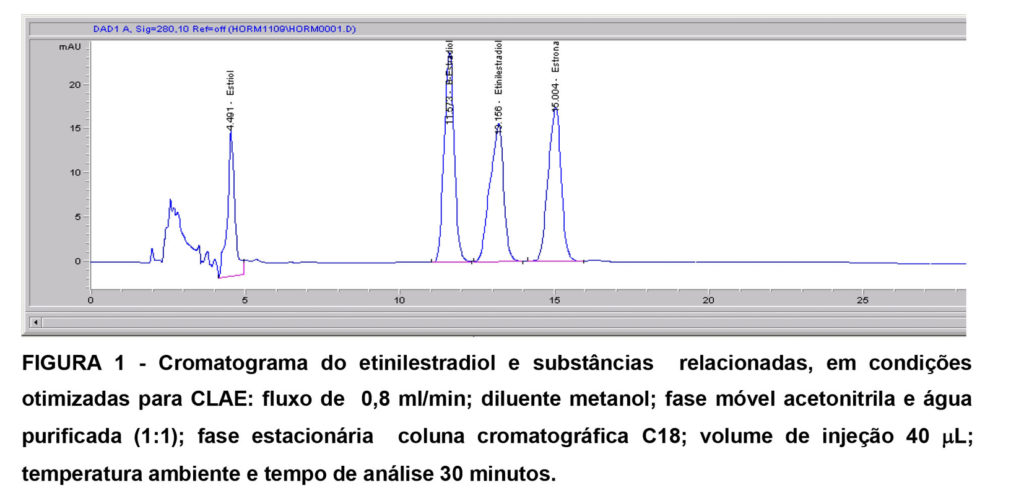
Após a realização de vários testes, obteve-se as condições otimizadas para as análises por CLAE: fluxo da fase móvel de 0,8 ml/min; fase móvel metanol grau HPLC e água purificada (50:50); fase estacionária coluna cromatográfica C18; volume de injeção de amostras 40 µl; temperatura ambiente e tempo de análise 30 minutos (FIGURA 1).
De acordo com o cromatograma obtido (FIGURA 1), os tempos de retenção destes hormônios estriol, 17b-estradiol, 17a-etinilestradiol, e estrona foram de 4,491 min, 11,513 min, 13,158 min e 15,004 min, respectivamente.
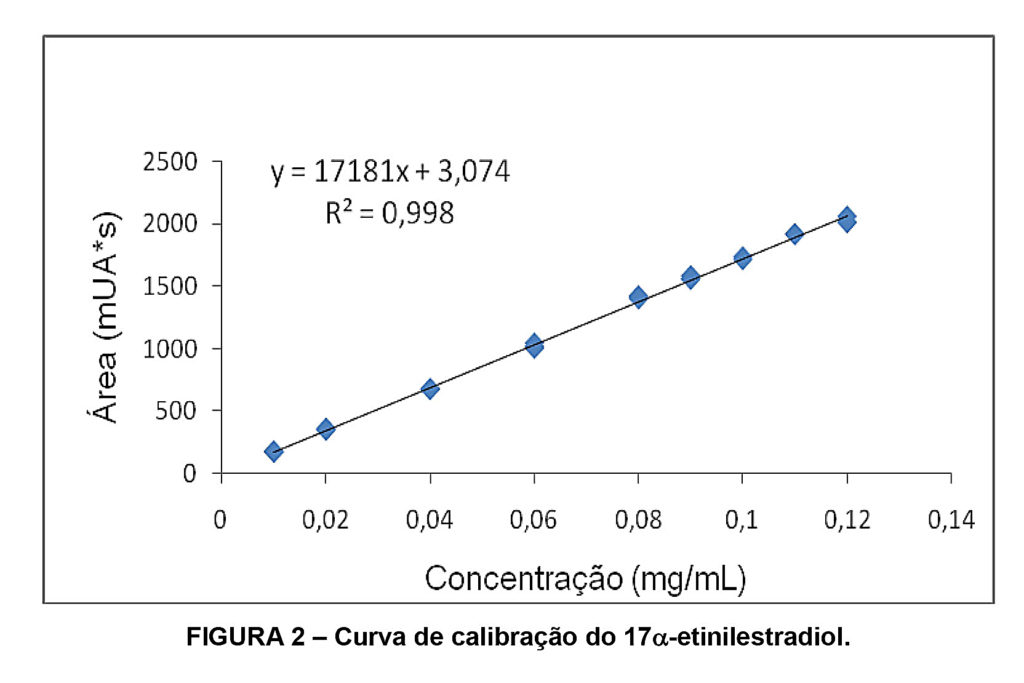
Para validar o método analítico, após definidas as condições de análise, construiu-se uma curva de calibração do 17a-etinilestradiol a partir das áreas dos picos nos cromatogramas obtidos para este hormônio após as injeções das soluções metanólicas de concentrações de 0,02 mg/mL a 1,2 mg/mL em triplicata (FIGURA 2). A obtenção desta curva de calibração tem como finalidade determinar a concentração de 17a-etinilestradiol presente em amostras analisadas contendo este hormônio, a partir dos valores das áreas dos picos obtidas nos cromatogramas.
A linearidade do sistema cromatográfico para o hormônio 17a-etinilestradiol foi verificada nas condições cromatográficas estabelecidas, a partir da curva de calibração construída na faixa de concentração de 0,2 a 1,2 mg/mL, obtendo-se um coeficiente de correlação (R2) igual a 0,998 que é bastante satisfatório.
.
CONSIDERAÇÕES FINAIS
De acordo com o cromatograma da mistura de hormônios e da curva de calibração do 17a-etinilestradiol obitidos, verificou-se que a metodologia desenvolvida para o sistema cromatográfico CLAE, pode ser utilizada para análises de amostras contendo o hormônio 17a-etinilestradiol e seus correlatos 17b-estradiol, estriol e estrona com boa resolução e confiabilidade. Além disso, o método analítico demonstrou-se eficiente e promissor para as análises das reações de degradação oxidativa do 17a-etinilestradiol já que permite identificá-lo e quantificá-lo nas amostras injetadas. A partir deste estudo, é possível analisar o hormônio 17a-etinilestradiol e seus produtos de degradação em condições adequadas, para avaliar as possíveis substâncias formadas e, posteriormente, separar e identificar cada produto formado, observando sua reatividade e seu impacto no meio ambiente.
.
REFERÊNCIAS
ANVISA- Agência Nacional de Vigilância Sanitária. Manual de Boas Práticas em Biodisponibilidade. Brasília: ANVISA, 2002, 2 v.
.
BIESAGA, M.; PYRZYNSKA, K.; TROJANOWICZ, M. Porphyrins in analytical chemistry. A review.Talanta v. 51, 209-224, 2000.
.
BILA, D. M; DEZOTTI, M. Fármacos no ambiente. Rio de Janeiro, v. 26, 2003.
.
COLLINS, C. H. ; BRAGA, G. L. ; BONATO, P. S. Introdução a métodos cromatográficos. 7. ed. São Paulo: Unicamp, 1997.
.
GROVES, J. T.; NEMO, T. E.; MEYERS, R. S. Hydroxilation and epoxidation catalyzed by iron-porphine complexes. Oxigen transfer from iodosylbenzene. J. Am. Chem. Soc. v. 101, 1032-1033, 1979.
.
HUANG, J.-Y.; LI, S.-J.; WANG, Y.-G. Selective oxidation of glycosil sulfides to sulfoxides with sodium hypochlorite and catalyzed by metalloporphyrins. J. Carbohydr. Chem. v. 29, 142-153, 2010.
.
MAKARSKA, M.; RADZKI, St.; LEGENDZIEWICZ, J. Spectroscopic characterization of the water-soluble cationic porphyrins and their complexes with Cu(II) in various solvents. J. Alloys Compd. v. 341 (1-2), 233-238, 2002.
.
MANSUY, D. A brief history of the contribution of metalloporphyrin models to cytochrome P450 chemistry and oxidation catalysis. C. R. Chimie v. 10, 392-413, 2007.
.
MEUNIER, B. Metalloporphyrins as versatile catalysts for oxidation reactions and oxidative DNA cleavage. Chem. Rev. v. 92 (6), 1411-1456, 1992.
.
MILGROM, L. R. The colors of life: an introduction to the chemistry of porphyrins and related compounds. New York: Oxford Academic Press, Oxford, p. 249, 1997.
.
PICKERING, A. D.; SUMPTER, J. P. Comprehending endrocrine disrupters in aquatic environments: additional projects arose from a three-year, multinational, multidisciplinary research program in the European Union. Environmental Science Technology, Easton, v. 1, p. 331-336, 2003.
.
THORPE, K. L.; CUMMIGS, R. I.; HUTCHINSON, T. H.; SCHOLZE, M.; BRIGHTY, G.; SUMPTER, J. P.; TYLER, C. R. Relative potencies and combination effects of steroidal estrogens in fish. Environmental Science & Technology, Easton, v. 37, p. 1142-1149, 2003.
.
NOTAS
1-Discentes do curso de Farmácia, alunas de Iniciação Científica do Centro Universitário Newton Paiva.
2-Discente do curso de Ciências Biológicas, aluno de Iniciação Científica do Centro Universitário Newton Paiva.
3-Colaborador da pesquisa, aluno de Doutorado da UFMG.
4-Colaborador da pesquisa, Docente da Faminas.
5-Colaboradores da pesquisa, Docentes da UFMG.
6-Colaborador da pesquisa, Docente do Centro Universitário Newton Paiva.
7-Coordenadora da pesquisa, Docente do Centro Universitário Newton Paiva.